- 耳たこ化学基礎「イオンとイオン結合」の暗記ページです。
- 四角い枠をクリックすると解答が表示され、下のボタンで一括表示・非表示の切替ができます。
- 耳たこ音読では音声ファイルを再生して要点を音読します。通学時間などのスキマ学習に最適です。
- 目次をクリックすると各セクションへ移動します。
イオンの形成
耳たこ音読|イオン
音声を再生して要点を音読しよう。耳たこになるまで、くり返し聞いて声に出すのが効果的!
ナレーション 音読さん
原子が粒子を失ったり、得たりすると用語を帯びて粒子となる。原子1個からなるイオンをイオンの種類、2個以上の原子が結合した粒子からなるイオンをイオンの種類という。
粒子の少ない原子は、電子を用語して用語となる。粒子の多い原子は、電子を用語用語となる。放出または受け取った電子の数をイオンの用語という。18族の分類名は価電子が個数でイオンになりにくい。
単原子イオンの用語は、用語がもっとも近い分類名と同じ電子配置となる。
単原子イオンには、H⁺、ヘリウムHeと同じ電子配置のLi⁺、ネオンNeと同じ電子配置のO²⁻、F⁻、Na⁺、Mg²⁺、Al³⁺、その他にS²⁻、Cl⁻、K⁺、Ca²⁺、Br⁻、I⁻、Ag⁺、Cu²⁺、Fe²⁺、Fe³⁺などがある。
多原子イオンには、NH₄⁺、H₃O⁺、OH⁻、NO₃⁻、HCO₃⁻、SO₄²⁻、CO₃²⁻、PO₄³⁻などがある。
イオンの種類
原子1個からなるイオンをイオン、2個以上の原子が結合した粒子からなるイオンをイオンという。
■ 陽イオンと陰イオン
価電子の多少原子
電子を受取or放出
価電子の多少原子
電子を受取or放出
価電子が2個
価電子が3個
価電子が7個
※18族の分類名。
単原子イオンの電子配置
■ 陽イオンの電子配置
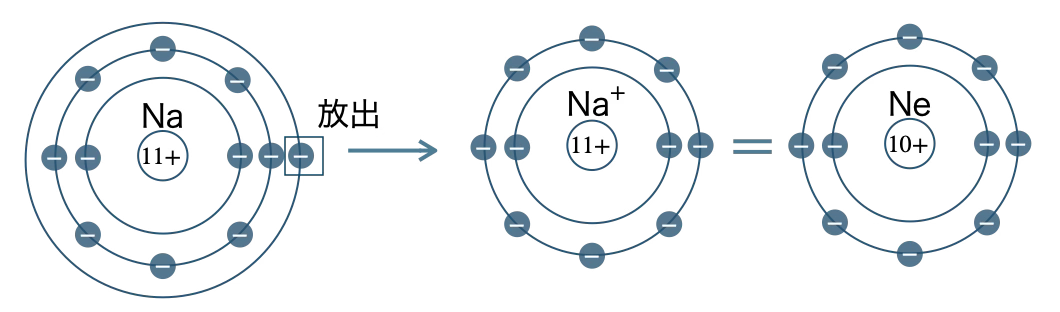
■ 陰イオンの電子配置
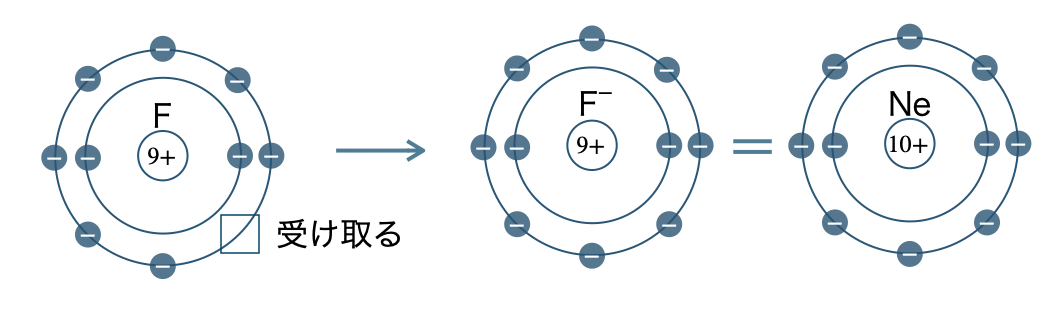
イオンの名称
陽イオンは命名法で遷移元素では命名法、陰イオンは命名法となる。
■ 多原子イオンの名称
イオンの生成とエネルギー
耳たこ音読|イオン化エネルギーと電子親和力
音声を再生して要点を音読しよう。耳たこになるまで、くり返し聞いて声に出すのが効果的!
ナレーション 音読さん
電子個数を失って価数+イオンとなるのに必要なエネルギーを用語という。周期表では、位置に行くほどイオン化エネルギーが大きくなり、イオンの種類になりにくくなる。元素名が最大である。
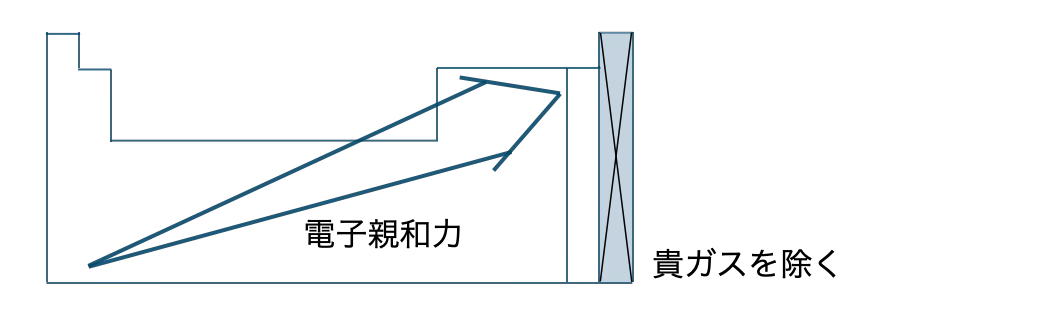
電子個数を受け取って価数+イオンになるときに放出するエネルギーを用語という。周期表では、分類名を除いて位置に行くほど電子親和力が大きくなり、イオンの種類になりやすくなる。
イオン化エネルギーと電子親和力

イオン化エネルギーが大小ほど、イオンになりにくくなる。
周期表では、右上に行くほどイオン化エネルギーが大小なり、イオンになりにくくなる。元素記号が最大となる。
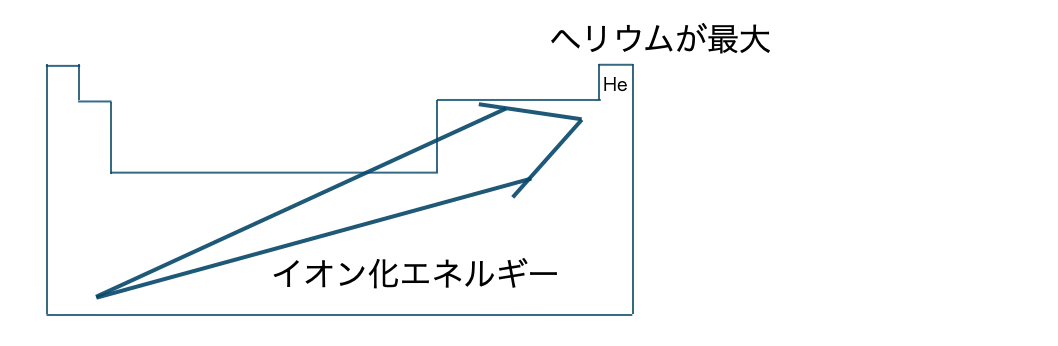
■ 陰イオンと電子親和力

電子親和力が大小ほど、イオンになりやすくなる。
周期表では、貴ガスを除いて右上に行くほど電子親和力が大小なり、イオンになりやすくなる。
原子とイオンの大きさ
耳たこ音読|原子とイオンの大きさ
音声を再生して要点を音読しよう。耳たこになるまで、くり返し聞いて声に出すのが効果的!
ナレーション 音読さん
用語元素では、周期表の位置にいくほど原子の大きさは大小なる。用語の元素では、周期表の位置にいくほど原子の大きさは大小なる。
原子は、用語になると原子の大きさは大小なり、用語になると原子の大きさは大小なる。
同じ用語をとる用語では、用語が多いほど(用語が大きいほど)、イオンの大きさは大小なる。
原子の大きさ
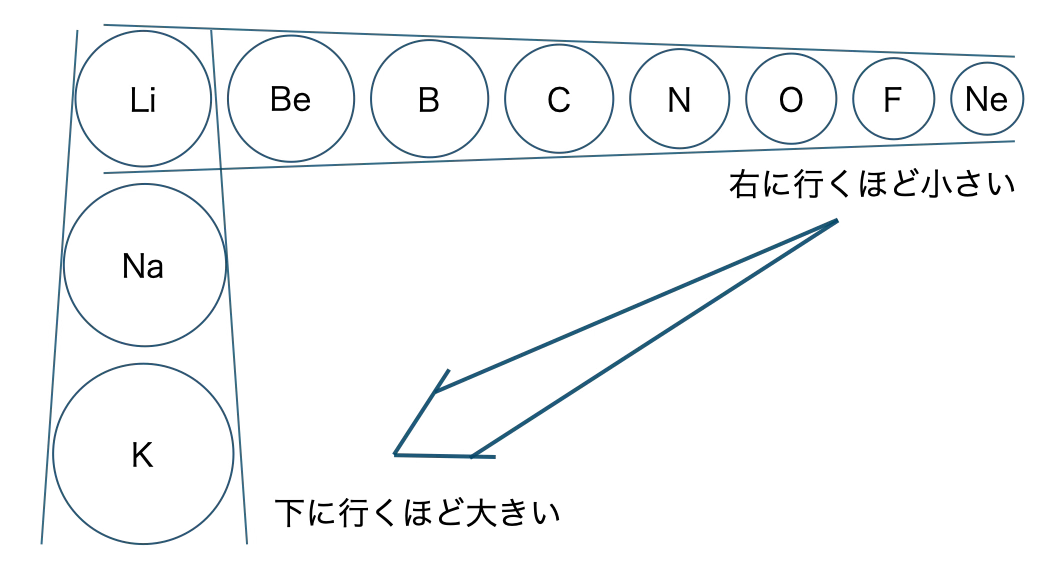
同周期の元素では、周期表の右にいくほど(用語が大きいほど)、原子核の正の電荷が増えて、より電子を引き付ける。これより、原子の大きさは大小なる。
イオンの大きさ
イオンになると電子殻が内側になるので、原子の大きさは大小なる。
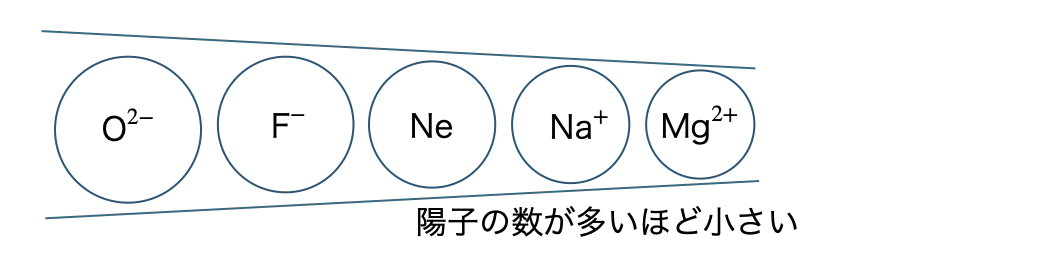
同じ電子配置をとるイオンでは、粒子の数が多いほど(原子番号が大きいほど)、原子核の正の電荷が増えて、より電子を引き付ける。これより、イオンの大きさは大小なる。
イオン結合とイオン結晶
耳たこ音読|イオン結合とイオン結晶
音声を再生して要点を音読しよう。耳たこになるまで、くり返し聞いて声に出すのが効果的!
ナレーション 音読さん
用語と用語の間に働く○○力(○○力)による結合を結合名という。
イオン結合によってできる結晶を結晶名といい、融点は高低、硬度は高低が性質。結晶では電気を通す?が、液体や状態では通す?。水に溶けやすい?ものが多い。
イオンからなる物質や金属、結晶名などを最も簡単な用語で表した式を用語という。
組成式は、化合物全体で電気的に性質になるように、用語を決める。
NaCl、Mg(OH)、AgNO₃、NaHCO₃、Al₂O₃、Ca₃(PO₄)₂などがある。
イオン結合
■ イオン結晶
融点は高低硬度は高低がもろい。結晶では電気を通す?が、液体や水溶液では通す?。水に溶けやすさものが多い。
組成式
イオンからなる物質の組成式は、化合物全体で電気的に用語になるように、イオンの割合を決める。
① 陽イオンの価数 × 個数=陰イオンの価数 × 個数となるように、それぞれの個数を決める。
Ca²⁺とCl⁻では、Ca²⁺1個とCl⁻2個となる。
② 陽イオン+陰イオンの順番で表し、右下にイオンの数を書く。(1個は省略する。)
Ca²⁺1個とCl⁻2個より、CaCl₂となる。
(例外)酢酸イオン CH₃COO⁻ のときは順番が逆になる。
→ CH₃COONa 酢酸ナトリウム
③ 名称は、名称+名称の順番に読む。ただし、「イオン」や「物イオン」は省略する。
CaCl₂では塩化カルシウムとなる。



